Bu bir felsefe sorusundan ziyade bir fizik sorusudur. Yaşayan tüm canlılar gibi siz de bir açık sistemsiniz. Yani bu ortam ile hem madde hem de enerji alışverişinde bulunuyorsunuz demek. Örneğin, yemekteki kimyasal enerjiyi alıyorsunuz ve etrafınızda hareket halinde bulunup işlerinizi görüyorsunuz, konuşuyorsunuz, yürüyorsunuz ve nefes alıyorsunuz.
Termodinamikte 3 tür sistem bulunmaktadır: açık, kapalı ve izole.
Açık sistem: Ortam ile hem enerji hem de madde alışverişi yapabilen sisteme açık sistem denir. Set üstü ocak açık sisteme bir örnektir. Çünkü ısı ve su buharı havada kaybolur.
Kapalı sistem: Diğer yandan bu sistem ortam ile sadece enerji alışverişi yapabilir, madde değil. Eğer bir önceki örneğin üzerine kapağı sıkıca kapatılmış bir çaydanlık koyarsak bu kapalı sisteme bir örnek olur.
İzole (Ayrık) sistem: Bu sistem ise ortam ile ne enerji ne de madde alışverişi yapamaz.
Termodinamik, ısı ve diğer enerji formları arasındaki ilişkilerle ilgilenen fizik dalıdır. Özellikle termal enerjinin diğer enerji türlerine nasıl dönüştüğünü ve bunun maddeleri nasıl etkilediğini açıklar
Termodinamikte 4 tane yasa yer almaktadır. Bu yasalar termodinamikte 0. , 1. , 2. ve 3. Yasalar olarak anılır. Bunun nedeni 1. Yasa oluşturulduktan sonra bilim insanları ondan da daha temel olan bir gerçeği keşfettiklerinde küçük bir oyun yaparak bu daha temel olan yasayı 1. Yasanın önüne 0. Yasa diyerek koymuşlardır. Hadi gelin bu yasaların ne olduklarını birlikte inceleyelim.
1.) Termodinamiğin 0. Yasası
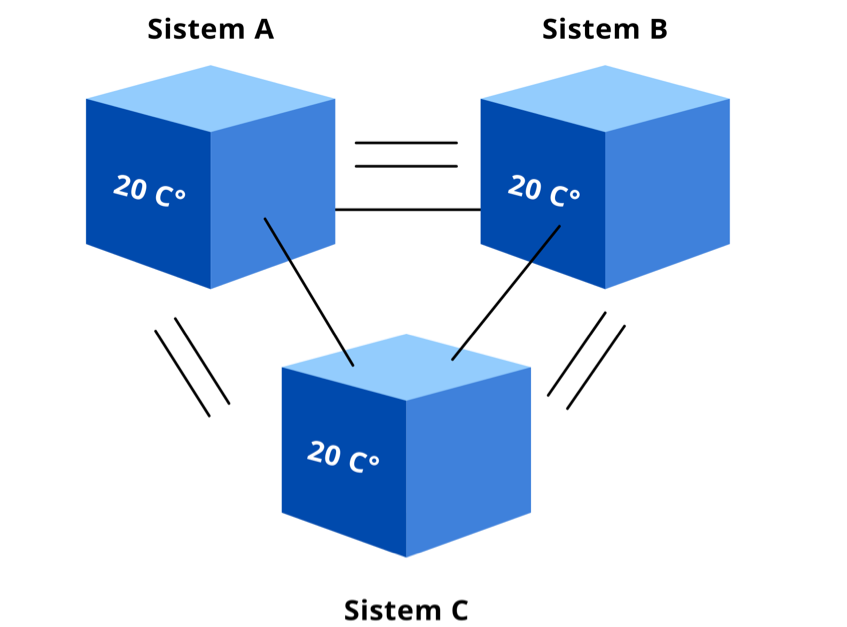
Sıfırıncı yasaya göre eğer iki ayrı sistem üçüncü bir sistem ile termodinamik dengedeyse o zaman o iki sistem de birbiri ile termal dengededir.
2.) Termodinamiğin 1. Yasası
Termodinamiğin birinci yasası evrendeki toplam enerji miktarı ile ilgilidir. Bu yasa özellikle evrendeki toplam enerji miktarının değişmediğini vurgular. Bir başka deyişle Termodinamiğin birinci yasası bize enerji yoktan var edilemez ve var olan enerji yok edilemez demektedir. Bu enerji yalnızca ya dönüşebilir ya da başka bir objeye aktarılabilir.
3.) Termodinamiğin 2. Yasası
İlk bakışta termodinamiğin birinci yasası çok harika görünebilir. Eğer enerji asla yaratılamıyor ya da yok edilemiyorsa o zaman bu da enerjinin sadece tekrar ve tekrar geri dönüştürüldüğü anlamına geliyor değil mi?
Şeey… Hem evet hem hayır. Enerji yoktan var edilemez ya da yok edilemez ancak kullanışlı halden daha az kullanışlı hale geçebilir. Bir başka deyişle, her gerçek dünyadaki enerji aktarımında ya da dönüşümünde enerjinin bir kısmı kullanılamaz bir hale gelmektedir (iş görmeye uygun olmayan). Çoğu zaman bu kullanılamaz enerji ısı halinde olur.
Eğer ısı iş görmüyorsa o zaman tam olarak ne yapıyor? İş görmeyen ısı doğrudan evrenin dağınıklığını (düzensizliğini) arttırmaktadır.
- Entropi ve Termodinamiğin 2. Yasası
Bir sistemdeki dağınıklık ya da düzensizlik miktarına onun Entropisi denir. Bildiğimiz üzere her enerji aktarımı sırasında enerjinin bir kısmı kullanılamaz hale (örneğin ısı) gelmektedir. Bu iş görmez ısı evrenin düzensizliğini artırır.
Her enerji aktarımı evrenin entropisini artırır ve iş yapmak için bulunan mevcut, kullanılabilir enerji miktarımızı azaltır.
4.) Termodinamiğin 3. Yasası
3. yasa entropi miktarını ölçebilmek için mutlak bir referans noktası sağlar.
“Bir sistemin sıcaklığı mutlak sıfıra (-273.15 °C, yani 0 Kelvin ) yaklaştıkça sistemdeki entropi miktarı da minimuma yaklaşır. ”
Genellikle 0K’de entropi değeri de 0 olur. Ancak bazı durumlarda yine de sistemde küçük bir miktar artık entropi olabilir.
KAYNAK: